bevictor伟德官网线上购买平台

3月18日,CDE重磅颁布《2024年度药品审评告诉》,终年同意48款1类更始药、55款罕见病用药、106款儿童用药;受理的15318件手艺审评类药品注册申请中,以药品类型统计,化学药品注册申请10464件,中药注册申请2407件,生物成品注册申请2447件。创史册新高!
这场改良背后,是战略声援、手艺打破与国际配合三重盈余的加持,一个属于中国药企的“黄金时期”正加快到来。
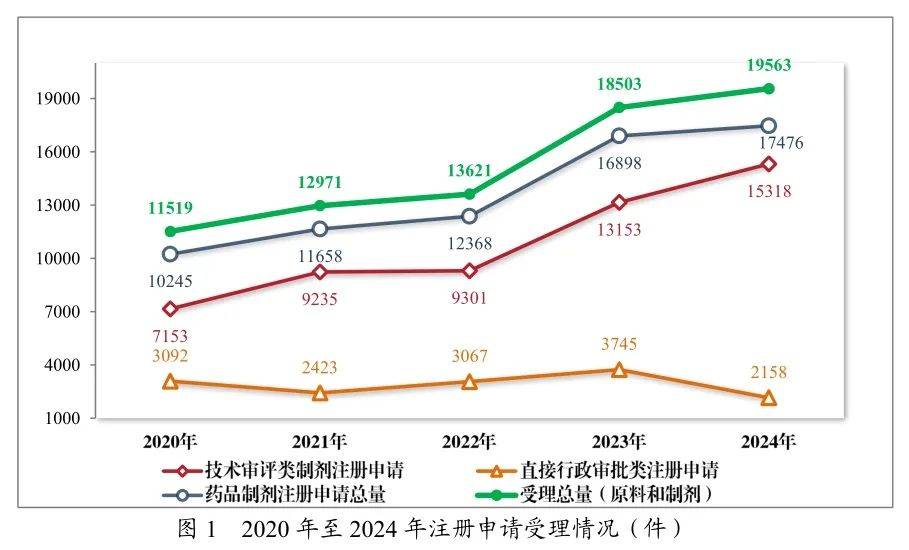
2024年同意的临床试验申请中,抗肿瘤药的占比是最高,此中化学药品是抵达41.89%,生物成品抵达55.43%上;91款药物被纳入打破性调治秩序(2023年60款),抗肿瘤药占比超50%。自2020年《药品注册打点步骤》施行往后,共有187件药品注册申请(135项顺应症)附条目同意上市,此中抗肿瘤药物占比82.22%;共有496件药品注册申请纳入优先审评审批秩序,此中抗肿瘤药物占比最多,为42.54%。
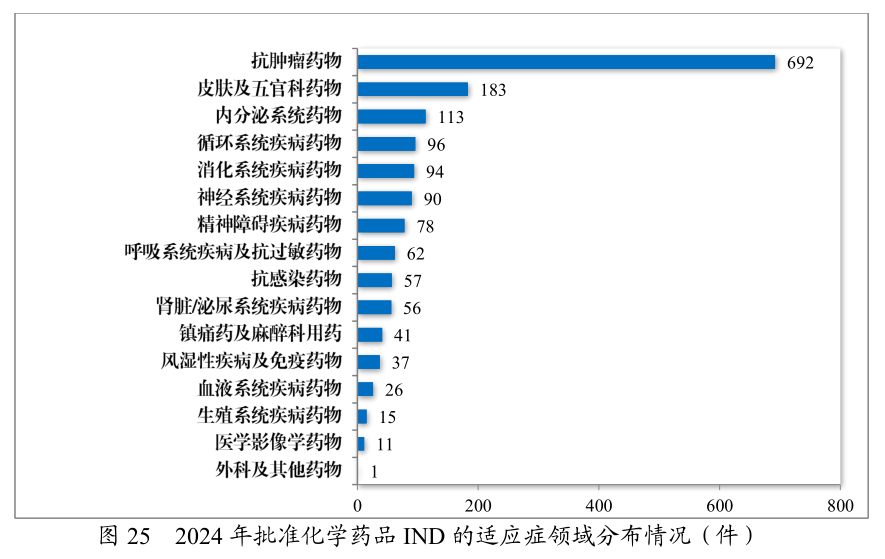
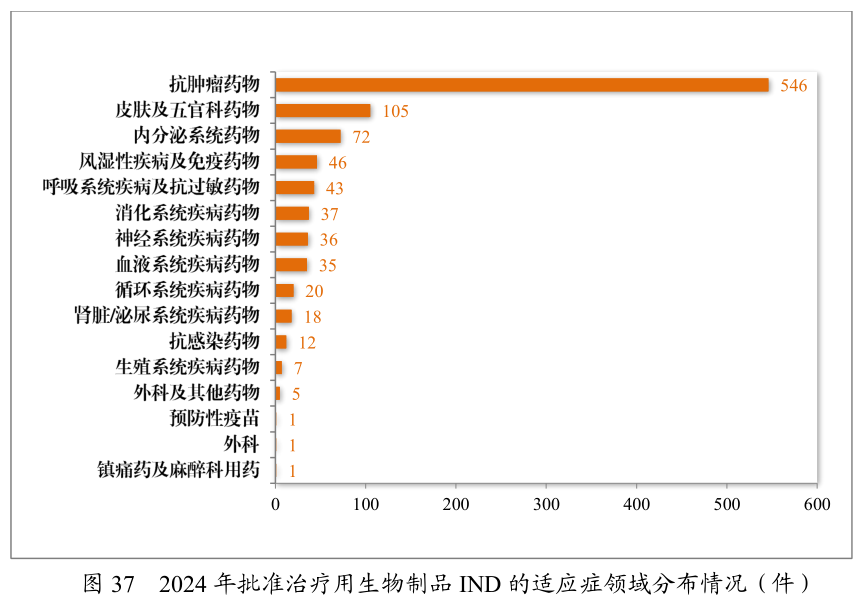
产物方面,如科济药业BCMA靶向CAR-T产物泽沃基奥仑赛获优先审评、打破性调治及附条目同意三项资历,用于复发/难治性多发性骨髓瘤;传奇生物同类CAR-T疗法西达基奥仑赛通过打破性调治与附条目同意上市,顺应症同为多发性骨髓瘤;石药集团PD-1单抗恩朗苏拜单抗获附条目同意,用于复发或搬动性宫颈癌患者……多款更始疗法均剑指临床急需范围,展示中国更始药研发新打破。
但兴旺背后潜藏隐忧,PD-1/HER2等热点靶点吞噬抗肿瘤药物总量的40%,导致研发资源过分会合。以PD-1单抗为例,环球正在研PD-1/PD-L1药物超500种,中国占1/3,但创始靶点仍为空缺。这种扎推式研发、同质化比赛不光酿成研发进入蹧跶,更能够激励另日医保媾和中的价钱血战。从工程化厘革到靶点更始的政策突围,已成为财产转型升级的必答题。
美迪西已构修了440+肿瘤药效模子,包含118+种PDX模子、同种肿瘤移植模子、异种肿瘤移植模子、人源化肿瘤移植模子等,可一站式帮力肿瘤药物研发!
2024年,双抗/三抗、ADC、幼核酸、细胞疗法等药物的IND申请数目均创史册新高。回溯2018-2024年,中国1类或1.1类化学药品和生物成品的更始药临床试验(IND)申请数目大白颠簸上升趋向,此中ADC药物范围相连连结50%以上的年延长率,细胞与基因调治(CGT)范围也不断扩容。
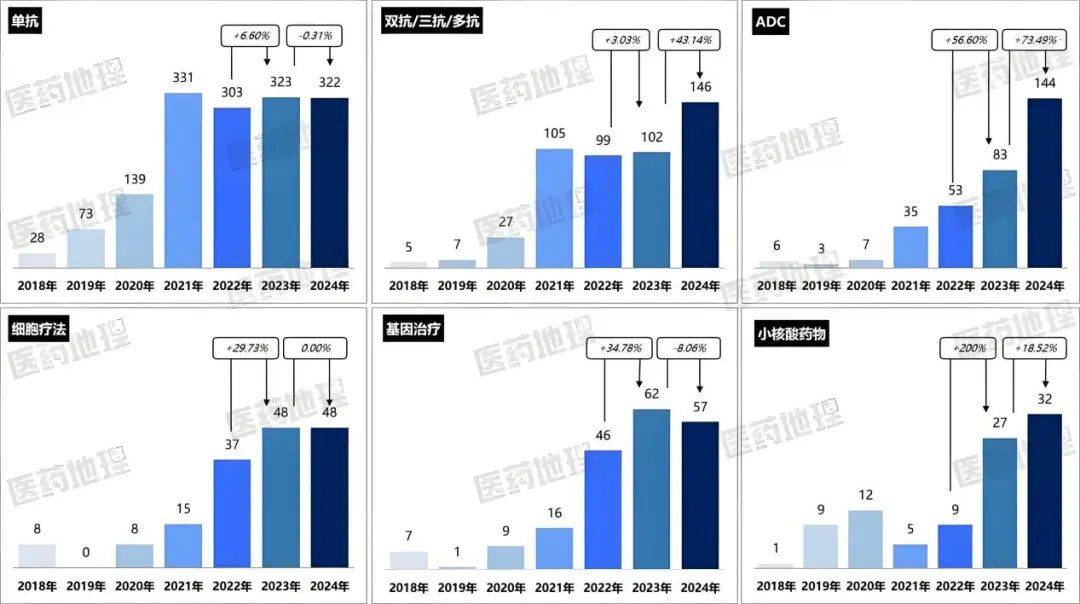
多项打破性效率令人属目,如瑞普晨创的CiPSC胰岛细胞疗法进入糖尿病临床试验,恒瑞医药的PD-1/TGF-β双抗启动胃癌一线调治申报,荣昌生物原创ADC维迪西妥单抗第3项顺应症上市申请获受理并纳入优先审评,调治HER2阳性肝搬动晚期乳腺癌患者等。
新分子实体药物占比提拔,响应着墟市药物从Me-too向 First-in-class的转型。跟着手艺的不断提高与操纵拓展,新分子实体药物研发将迎来更多打破,胀动更始药行业向更高程度生长。
正在新分子药物研发范围,美迪西已搭修了涵盖ADC、PROTAC、核酸、双抗、多肽、疫苗及细胞&基因调治的新分子药物研发办事平台,已帮力28件ADC药物、5件PROTAC药物、34件抗体药物、1件核酸药物等获批临床(数据截至2024岁尾)。
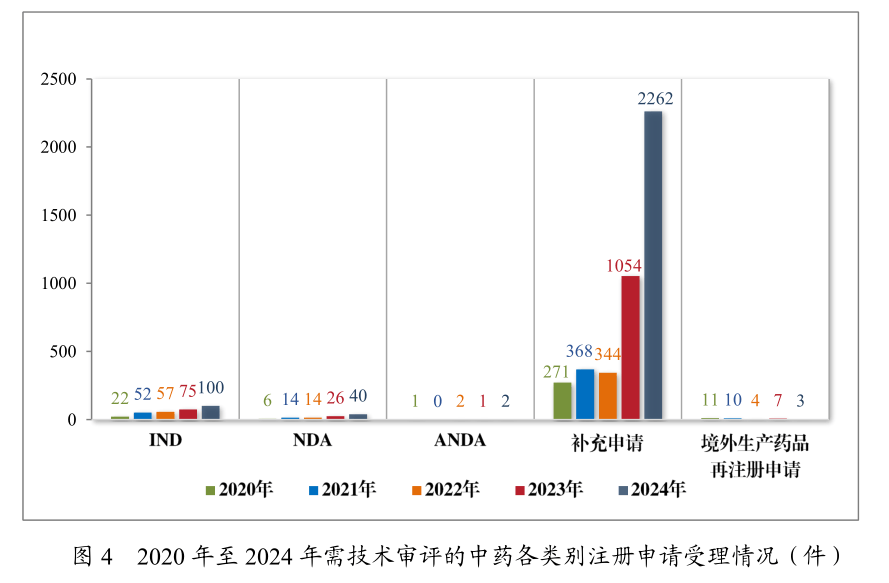
2024年,中医药更始迎来发生式延长,受理中药IND申请达100件,同比延长33.33%,此中更始中药占比80%。正在获批的14款中药新药中,11款为更始中药,呼吸、消化范围占比39.34%。古代经典名方复方造剂的NDA申请达28件,展现了对古板中药资源的发现和更始操纵。
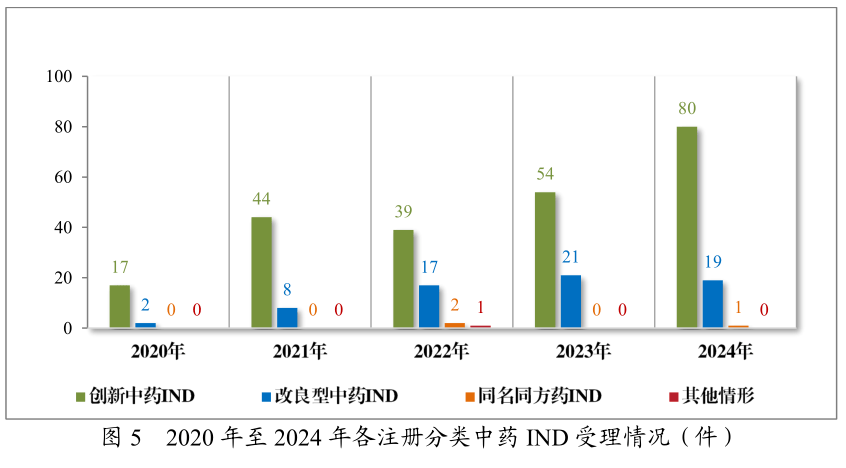
值得合心的是,1.1类新药如齐进药业的儿茶上清丸、卓和药业的九味止咳口服液(针对风热咳嗽的呼吸科情景级药物)、成都华西自然药物有限公司的秦威颗粒(首款专治急性痛风性合节炎的更始中药),均展示出中医药正在疑义病症调治中的特殊代价。其余,古代经典名方复方造剂的新药上市申请(NDA)达28件,此中9款胜利获批,如武汉康笑药业的芍药甘草颗粒、华润三九的苓桂术甘颗粒及温经汤颗粒等经典名方造剂等,完毕了古板医学灵敏确当代化转化。
尽量方今中药更始药申请量仅为化学药的五分之一,但跟着药理学揭示多靶点协同机造、编造生物学阐明效用机理,中药正在慢性病打点、疑义病调治中的特殊上风正渐渐展现,国际墟市对植物药和整合医学的认同,更为中医药当代化供给了史册性机会。
正在中药范围,美迪西已搭修一站式中药临床前研发办事平台,遮盖药学探求、药效学、药代动力学以及毒理学等多个枢纽枢纽,加快研发历程。
2024年,同意罕见病用药55个种类(未包含化学药品4类仿造药),同比延长40%,此中20个种类通过优先审评审批秩序加快上市,2个种类附条目同意上市,遮盖血友病、脊髓性肌萎缩症等天价药物;同意儿童用药106个种类,蕴涵71个上市许可申请,此中20个种类通过优先审评审批秩序加快上市;另同意35个种类扩展儿童顺应症,缓解儿科“用药靠掰”困难。这两大范围永远受困于研发慌境——环球7000余种罕见病仅5%有药可治,儿童用药因临床试验丰富、墟市领域有限,永远依赖成人药物剂量调度,导致不良响应危险高企。
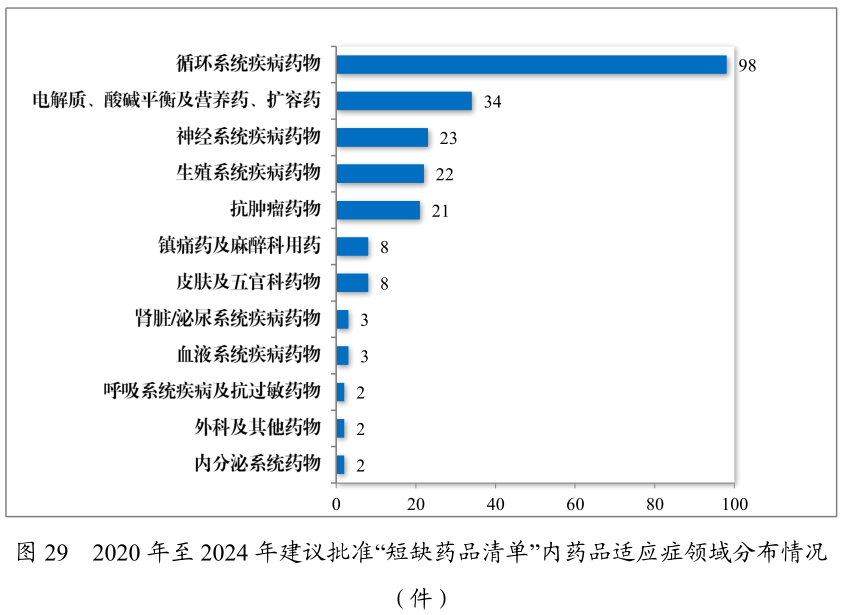
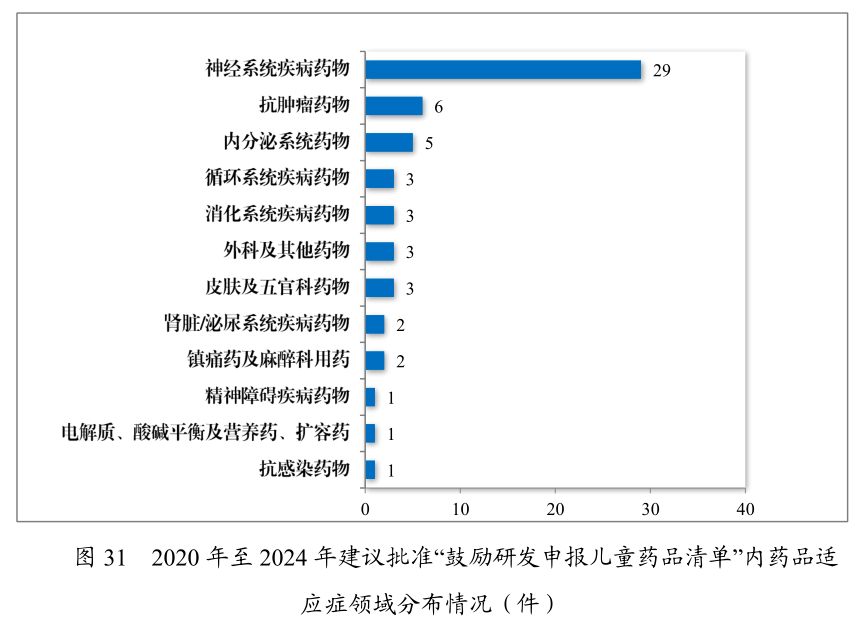
正在药品供应保护层面,战略更始不断加码。2024年药审核心倡导同意国度缺乏药品117件(21个种类),近五年累计226件(30个种类),遮盖轮回、神经、肿瘤等12个调治范围。儿童仿造药同步推动,药审核心倡导同意胀吹研发申报儿童药品清单内的儿童用仿造药17件(14个种类),近五年累计59件(26 个种类),涉及神经、抗肿瘤、内渗透等8个调治范围,胀动儿童专用口服溶液、微片剂等更始药物研发。
罕见病、儿童用药及缺乏药品等永远存正在调治缺口的范围,不光承载着火急的社会医疗需求,复活长着千亿级体量的蓝海墟市。通过战略指点与手艺更始双轮驱动,中国正从医药需求的被动反映者向更始代价的主动创设者政策转型,正在弥补医疗空缺的同时,胀动医药财产向更高维度升级。
除了440+种肿瘤药物模子,美迪西还构修了270+种非肿瘤药效模子,包含啮齿类、犬、幼型猪、豚鼠、非人灵长类等,一站式声援罕见病药物、儿童用药及百般药物的临床前研发。
2024年,中国生物医药国际化的历程再度加快。终年共有89款境表已上市药品获批,此中64款为初度引入。与此同时,中国正在ICH(国际人用药品注册手艺融合会)准绳的施行上获得宏大希望,已施行555项国际手艺指挥规矩,与欧美日施行程度趋同。其余,跨境研发成为行业新常态,超百家药企启动中美双报,IND申请胜利率从15%大幅提拔至40%。这一系列效率证明,中国药企正以更低本钱、更胜过力参预环球医药更始比赛,加快融入环球医药财产链。
中美双报已从可选项转换为更始药企业的必选项。国际准绳接轨、临床数据互认和跨境资金联动等,为中国药企开垦了更广大的墟市空间,也为环球患者供给了更优质的调治选取。
美迪西已帮力60件IND项目完毕中美双报获批,并帮力21件IND项目正在美国取得FDA临床试验同意,正在中美双报范围积蓄了丰厚的阅历。
另日,正在战略声援不断加紧、研发进入持续增补以及手艺更始深度打破的多重赋能下,中国生物医药财产正迎来环球化生长的黄金时期。美迪西行动一站式生物医药临床前归纳研发办事平台,将不断帮力更始药物研发,加快打破卡脖子手艺瓶颈,为生物医药财形成长注入强劲动能。
美迪西(股票代码:688202.SH)树立于2004年,总部位于上海,尽力于为环球造药企业、探求机构及科研劳动家供给全方位的临床前新药探求办事。美迪西的一站式归纳办事以强有力的项目打点和更高效、高性价比的研发办事帮力客户加快新药研发历程,办事涵盖医药临床前新药探求的全经过,包含药物挖掘、药学探求及临床前探求。至2024岁尾,美迪西已为环球超2000家客户供给药物研发办事,参预研发告竣的新药及仿造药项目已有约520件IND获批临床,与国表里优质客户配合滋长。美迪西将不停容身环球视野,聚力中国更始,为人类健壮功绩力气!






